THM 전구물질 및 소독부산물, 색도, 암모니아성 질소, 음이온 계면활성제
THM 전구물질 및 소독부산물
1974년 Rook와 Bellar에 의해 THM(Triholomethane)은 음용수에서 확인되고 이들은 염소소독과 연관성이 깊다고 발표되었는데, 수돗물중에 발생하는 THM은자연에 존재하는 유기착색성분인 휴민질(Humin)이나 그것과 유사한 유기물인 전구물질(Precursor)과 전염소처리나 소독을 위해 투입하는 염소와의 반응으로생성된다.
THM의 4가지 화합물(Cholorform, Bromodichloromethane, dibromochloromethane, Bromoform) 중에서 클로로포름(CHCl3)이 일반적으로 가장 큰 비중을차지하고, 이들 화합물을 합하여 총트리할로메탄(Total Trihalomethane, TTHM)이라고 정의하며 발암성 물질인 것으로 확인되었다.
완속여과방식에서는 미생물군에 의해 형성된 생물여과막에 의해 일부 유기화합물을 산화 또는 분해하나, 휴민질 등의 안정한 천연색도성분에 대해서는 그다지효과가 높지 않기 때문에 THM 전구물질의 제거도 그다지 효과적이지 않다.
또한 원수 수질오염이 심화되면 급속여과방식을 적용한 표준정수처리공정에서는 전염소처리 등을 적용하기는 하지만 THM 전구물질의 억제효과의 폭이 그다지크지 않다. 이러한 경우에는 활성탄 처리나 오존처리 방법이 효과적인 것으로 알려져 있다.
색도
원수 중의 황색 성분은 부식질에 기인하는 것이 많으나, 철, 망간에 기인하는 것과 산업폐수의 혼입에 기인하기도 한다.
부식질로부터 유래하는 색도는 휴민산(Humic acid), 펄빅산(Fulvic acid)으로 구분되지만, 일반적으로 휴민산은 강산에서 불용성이고 분자량이 크므로 pH를낮게 하여 응집/침전하면 제거가 쉽게 된다. 반면, 펄빅산에 기인한 색도는 휴민산보다 분자량이 훨씬 적고 산과 염기에 대해 용해성이므로 표준정수처리공정으로처리하기 어려우므로 활성탄처리 또는 오존처리가 효과적인 것으로 알려져 있다.
암모니아성 질소
단백질 등의 질소를 포함한 유기물을 생물이 이용, 분해하여 배출되는 화합물의 대표적인 것이 암모니아성 질소이다.
일반적으로 원수에 함유된 농도에서는 건강상의 영향을 미치지 않으나, 저수지 등에서 부영양화가 진행될 경우 조류와 같은 미생물 번식의 원인이 된다.
수온이 낮은 겨울철에 암모니아성 질소를 산화하는 질산화 미생물의 활성도가 크게 감소하기 때문에, 일반적으로 암모니아성 질소의 농도가 높게 나타난다.
정수처리에 있어서는 유기물, 철, 망간 등의 산화와 함께 암모니아성 질소처리를 목적으로 전염소처리가 행하여져 왔으나, 휴민산류 등의 용해성 유기물질과염소가 반응하여 THM 생성에 큰 영향을 미친다.
암모니아성 질소농도가 낮은 경우에는, 완속여과공정과 같은 호기성 미생물에 의한 산화법이 신뢰성이 높다.
반면, 일정농도 이상에서는 생물처리가 효과적이지만 겨울철 수온이 낮을 때는 효과가 감소하여 적용에 어려움이 있다.
음이온 계면활성제
음이온 계면활성제는 가정하수, 산업폐수 등의 혼입에 의해 유래되며, 일반적으로 수도 원수에서는 주로 발포에 의한 장애를 일으킨다.
경성합성세제(Alkylbenzene sulfonate, ABS)는 일시 사용되었으나, 생물 분해성이 나쁘기 때문에 생물분해성이 좋은 연성합성세제(Linear Alkyl benzenesulfonate, LAS)로 바뀌어 사용되고 있다. 그러나 도시에서 인구증가와 합성세제 사용량의 증가로 유입 부하가 높아져 LAS가 분해되지 않고 잔류하게 되며, 특히 생물 분해속도가 낮은 겨울에 고농도로 유입되어 문제를 일으키고 있다.
고도정수처리공정
먹는물의 목표수질 달성을 위해 표준정수처리기술로는 불가능한 여러 가지 오염물질들을 처리하기 위한 대표적인 고도정수처리공정으로는 오존처리, 활성탄처리, 막분리, 생물학적 전처리 등을 들 수 있으며, 이 밖에도 해수담수화, 전기투석법 등이 있다.
이러한 고도정수처리 공정들은 표준정수처리공정에 단독적으로 추가되거나 그 효과를 향상시키기 위하여 조합된 형태로 구성될 수 있다.
오존처리 공정
19세기말 오존 살균력이 발견된 후, 독일에서 정수장에 파일럿(pilot) 플랜트를 설치하여 박테리아에 대한 살균효과를 검증한 바 있으며, 따라서 초기에는 살균제로서 도입되었다. 부수적으로 맛, 냄새 물질, 색도, 철 및 망간 등의 제거도 가능한 것으로 밝혀지면서 그 사용범위가 확대되어 왔다.
1970년대 THM이 발견된 이후부터, 오존 공정은 최근까지 상수원수의 오염심화와 오염물질의 다양화 추세, 먹는물 수질기준의 강화, 염소처리에 의한 소독부산물(DBPs) 발생 등의 복합적인 수질문제에 대응하여 조류제어 및 소독부산물을 제어할 목적으로 고도정수처리에 도입되고 있다.
크립토스포리디움에 의한 수질사고 이후, 소독제로서 오존에 대한 관심이 증가하였으며, 더욱이 오존은 살균효과가 우수하고 염소 소독과는 달리 THMs 등의 화합물을 생성시키지 않는 장점이 있다. 게다가, 강력한 산화력에 의해 페놀, ABS 등의 난분해성 유기물질의 분해․제거가 가능하고 THM 전구물질이나, 맛․냄새 등의
제거에도 매우 효과적이다. 또한, 유기물질의 성상을 변화시킨 후, 활성탄에 흡착시켜 제거하는 전처리 방법으로도 활용할 수 있어 소독부산물의 제어를 위한 생물활성탄(BAC)에 대한 전처리시설로서 적용되고 있다.
따라서 프랑스를 비롯한 유럽지역은 물론 미국을 포함한 북미지역에 오존처리공정이 급속도로 확산되었다.
반면, 오존처리 기술이 정수처리기술 분야에서는 조금 낯선 실정이고, 도입에 따른 과도한 소요비용, 현장생산에 따른 기술적인 문제점들이 있다.
또한, 오존의 강한 산화력에 의한 브로메이트(bromate, BrO3-), 클로레이트(chlorate, ClO3-), 알데하이드(aldehydes)와 같은 소독부산물들이 생성될 수 있으며, 이들에 대한 위해성 검증과 대책이 과제로 남아 있다.
출처 : 2004년 환경부 "고도정수처리 정책방향에 관한연구" 발췌
'수질관련용어' 카테고리의 다른 글
| 완속여과(Slow sand filtration) (1) | 2022.11.14 |
|---|---|
| 고도정수처리 및 문제시되는 먹는물의 오염물질 종류 (0) | 2022.11.14 |
| 오존과 염소의 소독력에 대한 상대적 비교 (0) | 2022.11.13 |
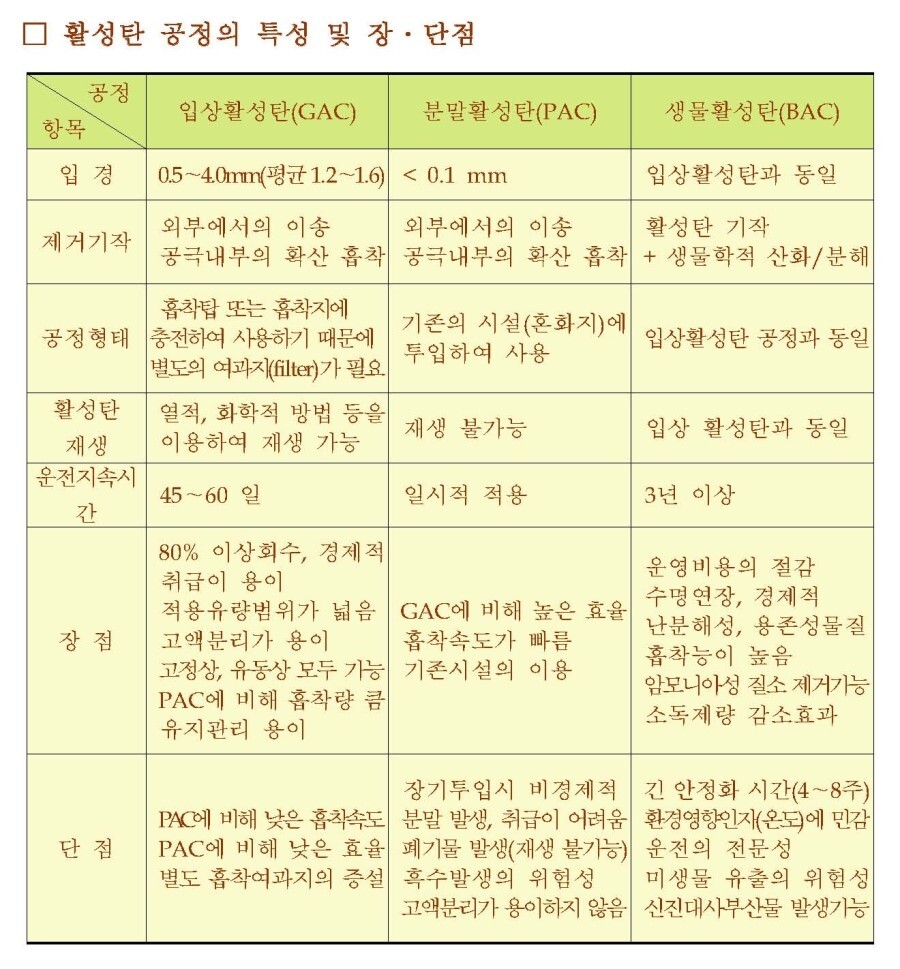
| 활성탄처리 공정 (0) | 2022.11.13 |
| 생물활성탄(Biological Activated Carbon, BAC),분말활성탄(Powdered Activated Carbon, PAC) (0) | 2022.11.13 |