반응형
pH값 변화에 따른 유리 잔류염소(Free Chlorine) 존재비율
유리 잔류염소
음용수의 정수처리나 방류수에 가장 많이 사용되고 있는 살균제는 염소이며, 염소는 1기압, 20℃에서 7,160mg/l 정도의 용해도를 나타내고 다음과 같이 대부분가수분해된다.
Cl2 + H2O ⇔ HOCl + H+ + Cl-(낮은 pH)
HOCl ⇔ H+ + OCl- (높은 pH)
pH 7 정도에서는 주입한 염소의 절반이 Cl-(살균 효과없음)으로 존재하고, 나머지 양중 대략 절반씩 HOCl와 OCl-로 존재하여 살균작용을 한다.
pH 10이상에서는 OCl-로 되어 HOCl은 나타나지 않는다. 낮은 pH에서는 HOCl의 생성이 많고, 높은 pH에서는 OCl-가 더 많이 존재한다.
이 두물질의 살균력은 HOCl이 OCl-보다 약 80배이상 강하다.
pH가 5이하에서는 Cl2의 형태로 존재한다. 염소가 수중에서 HOCl, OCl-로 존재할 때 이 염소를 유리염소 또는 유리잔류염소라 한다.
pH값 변화에 따른 유리잔류염소의 존재비율은 아래 그림과 같다.

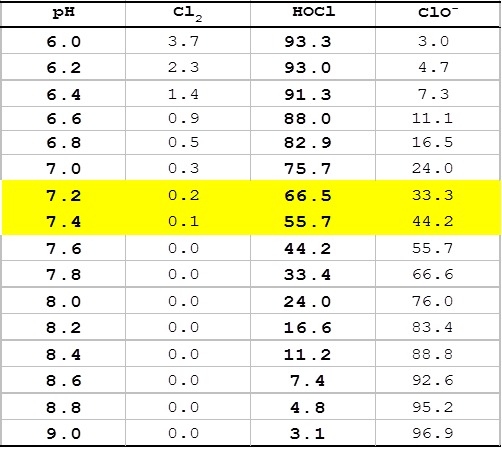
<pH값에 따른 유리잔류염소의 존재비율>
===> 출처 : 동화기술 <환경공학>, 관련업체 홈페이지 자료 및 인터넷 자료 정리

반응형
'수질관련용어' 카테고리의 다른 글
| pH 측정값이 계속하여 14pH를 가리키거나 범위를 벗어날 때는? (1) | 2022.09.18 |
|---|---|
| pH Meter가 자동보정이 안되는 경우에는? (0) | 2022.09.18 |
| PH 전극의 보관 및 유지보수 (0) | 2022.09.18 |
| 전극 보관 시 검사 항목 (0) | 2022.09.18 |
| pH 측정시스템의 전위란? (0) | 2022.09.18 |