갈바닉(Galvanic)DO전극 과 폴라로그래피(Polarography) DO전극 비교
| 갈바닉(Galvanic) | 폴라로그래피(Polarography) | |
| 측정 원리 |
양극과 음극의 다른 금속원소간의 내부 반응 으로부터 일정하지 않은 자체 바이어스 전압을 유도해 냅니다. 하지만, 대부분의 Galvanic 센서 는 전자 증폭 없이 전류계를 직접 작동시키는 충분한 정도의 전류를 만들어 내기 때문에 과도한 산소 소모가 문제가 됩니다.(과도한 물의 환원 작용으로부터 발생하는 offset 전류) |
DO 트랜스미터에서 공급된 제어 전압 원천으로부터 바이어스 전압을 유도합니다. DO 트랜스미터는 피드백 루프를 사용하여 정확한 전압 수준을 유지합니다. 센서가 제기능을 발휘하려면, 전류출력 정체 지점에서 음극 전위가 유지 되어야 합니다. Polarographic 산소 센서 사용 시, 산소 측정에는 675 mV 극성화 전압이 가장 적당합니다. |
| 장점 | 전극 교체 후 즉시 측정이 가능하다. 가격이 비교적 저렴하며 많이 보급 되어 있다. |
유속이 없는 물에서도 정확한 측정이 가능하다. 저농도의 경우에도 비교적 정밀한 측정이 가능하다. |
| 단점 | 유속이 미약한 액체에서는 측정이 곤란하거나 측정값에 대한 오차가 크다. |
초기 운전 시 및 재 전원 공급시 Polarizing 시간이 필요 하다(8-12시간). 정밀한 측정을 위하여 Zero Point 교정 이 별도로 필요하다. 비교적 가격이 비싸다. |
| Type | 전극의 Type에 따라 전극 교체형, 보충형 또는 충전 보수형으로 구분한다 |
전극의 Type에 따라 격막 및 내부액 교체형 및 무교체형으로 구분된다. |
| 수명 | 전극 교체형 : 6 ∼ 10개월 정도 보충형 전극 : 1년 정도 충전 보수형 : 2년 정도 |
교체형 : 2 ∼ 3년 정도 무교체형 : 2년 정도 |
| 전해액 | 전해액을 자주 보충 및 교체해 주어야 한다. | 전해액의 수명은 최대 6개월이며, 교체형의 경우 보충 및 교체해 주어야 한다. |
| Membrane | 다양한 재질로 된 격막은 손상여부를 확인해야 하고 파손 시 교체를 해주어야 한다. |
다양한 재질로 된 격막은 손상여부를 확인해야 하고, 파손 시 교체를 해주어야 한다. 기타 재질로 보강이 된 형태도 있어 장기간 사용이 가능하다. |
| 세척 | Galvanic Cell의 높은 용존 산소의 소비율로 인해 음극-양극을 빈번하게 세척하여 주어야 한다. |
격막이 파손되지 않으면 세척주기를 장기간으로 하여도 비교적 안정적인 측정이 가능하다. |
| 소모품 교체 | 일반적인 형태는 오링, 테프론 격막, 그리고 몸체를 포함한 복잡한 작업이 되며 시간이 많이 소요된다. |
하나의 격막단위로 되어 1분 이내에 교체가 가능하다. |
| 기능 사양 |
일반적으로 오·폐수처리장의 폭기조에서 많이 사용된다. |
발효 및 생물반응 공정 중 고온증기 살균, 고압 환경에 서도 사용이 가능하며, 오·폐수처리장 뿐만 아니라 식품, 음료, 의약 산업 등의 분야에도 응용된다. |
| 비용 측면 |
소모품의 비용은 상대적으로 저렴하지만, 자주 점검 및 교환을 하여야 하며, 또한 유지·보수 시 점검시간을 많이 필요로 하게 된다. |
소모품의 비용은 상대적으로 고가이나, Galvanic Cell에 비하여 소모품 및 전해액의 수명이 길어 장시간 안정 적인 측정이 가능하며, 유지보수 시 점검시간이 많이 소요되지 않는다. |
갈바닉 전극
용존산소 측정기는 제조회사에 따라 다소 차이가 있으나 원리는 모두 동일하다. 용존산소 측정기에 사용하는 전극을 격막전극(Membrane Electrode)이라고 하며,
구성으로는 격막, 은전극, 납전극, 전해액실, 침지셀 등으로 이루어져 있다.
갈바니 전지 방식은 납과 은의 전극이 전해질 층으로 덮여 있어 이 봉(Probe)을 시료 속에 담그면 산소분자와 다음과 같이 반응한다.
양극에서의 반응 :
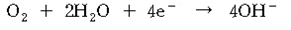
음극에서의 반응 :

납 전극에서 전자가 자유롭게 양극으로 이동하면서 시료 속의 산소분자는 격막을 통하여 양극 표면에서 전자를 잡아 환원 반응이 일어난다.
즉, 시료 속의 용존산소량에 비례하여 전류가 흐르게 된다.
폴라로그래픽 전극
음극(cathode)은 금이나 백금과 같은 비활성 금속을 사용하며 양극(anode)으로는 은을 이용한다.
Polarographic probe는 일정한 전압이 전극에 가해지면 은 전극이 편극 되고 음극에서 산소 이온의 환원이 일어나며 시료 내 산소의 부분압에 비례하여 전류가
발생한다. 반응은 다음과 같다.
산소는 전극 membrane을 통해 확산하고 음극 표면에서 hydroxyl ion으로 환원된다.
음극 O2 + 2H2O + 4e- → 4OH-
이 반응에 필요한 전자는 양극에서 다음과 같은 반응에 의해 제공된다. 전해질은 chloride 이온을 포함하기 때문에 Ag와 반응하여 전자를 발생시킨다.
양극 Ag + Cl- → AgCl + e-
시료 속의 용존 산소량에 비례하여 전류가 흐르게 된다.
'수질관련용어' 카테고리의 다른 글
| DO(용존산소)를 분석하는데 이용되는 2가지 방법 (0) | 2022.11.08 |
|---|---|
| 용존산소 교반속도(Sample speed) 영향에 대해서 (0) | 2022.11.08 |
| 도막 두께측정기,도금두께 측정기, 초음파 두께 측정기, 핀홀측정기, 부착력측정기 ,표면조도,광택계 품질계측기 소개 (0) | 2022.11.07 |
| GPS에 대해서 (0) | 2022.11.07 |
| 화학적 산소 요구량(COD)를 측정해야 하는 이유는? (0) | 2022.11.07 |
